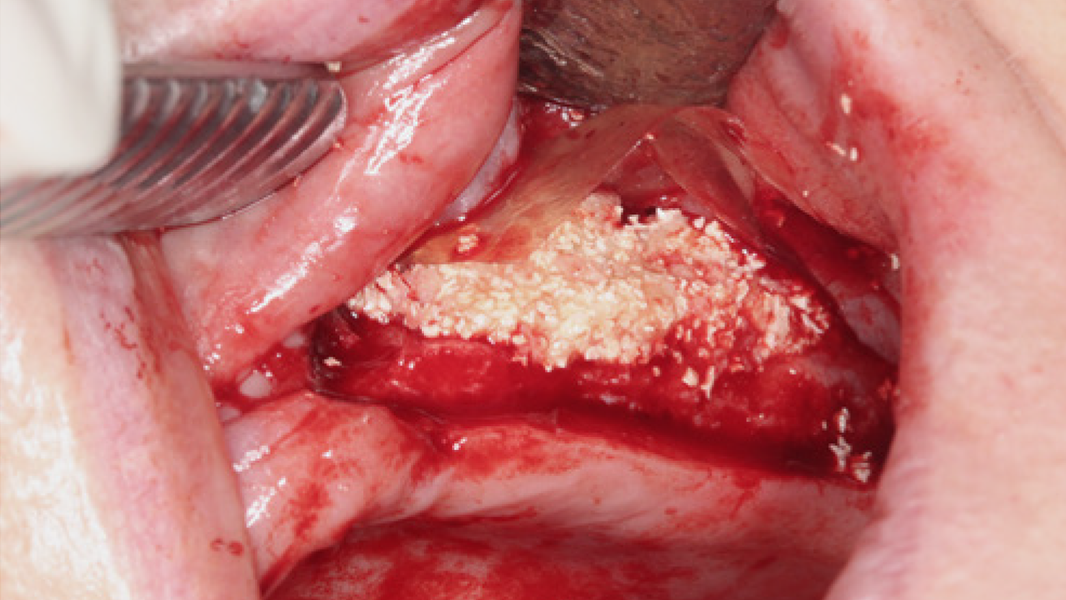
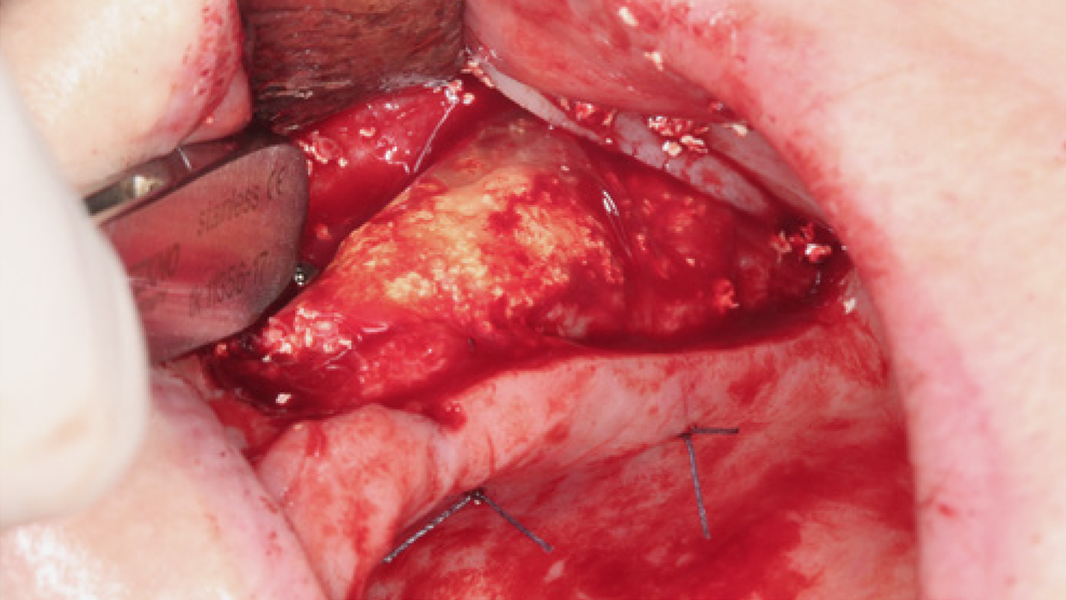
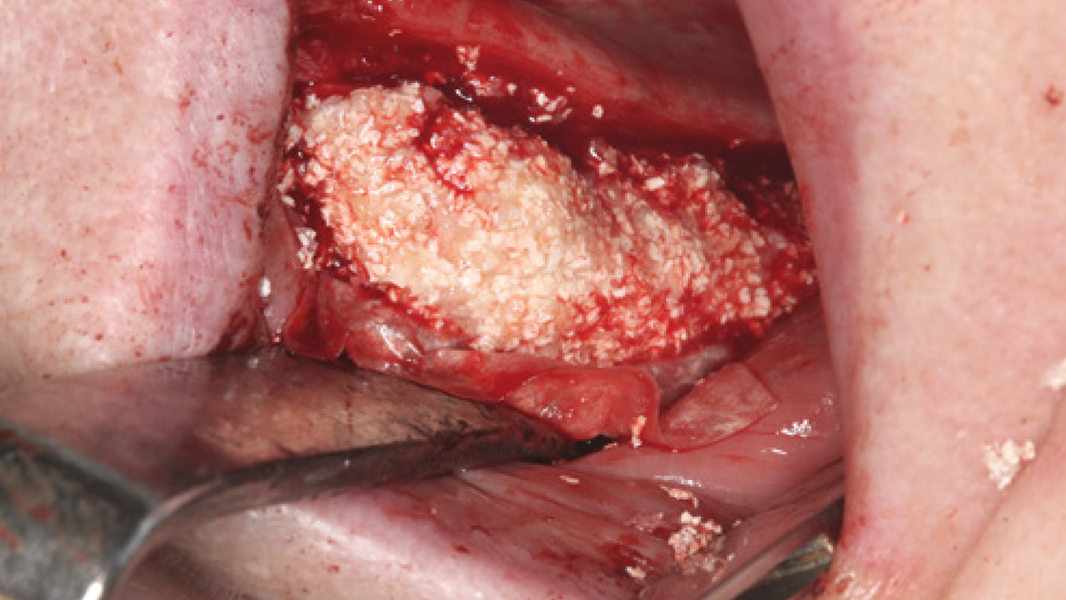
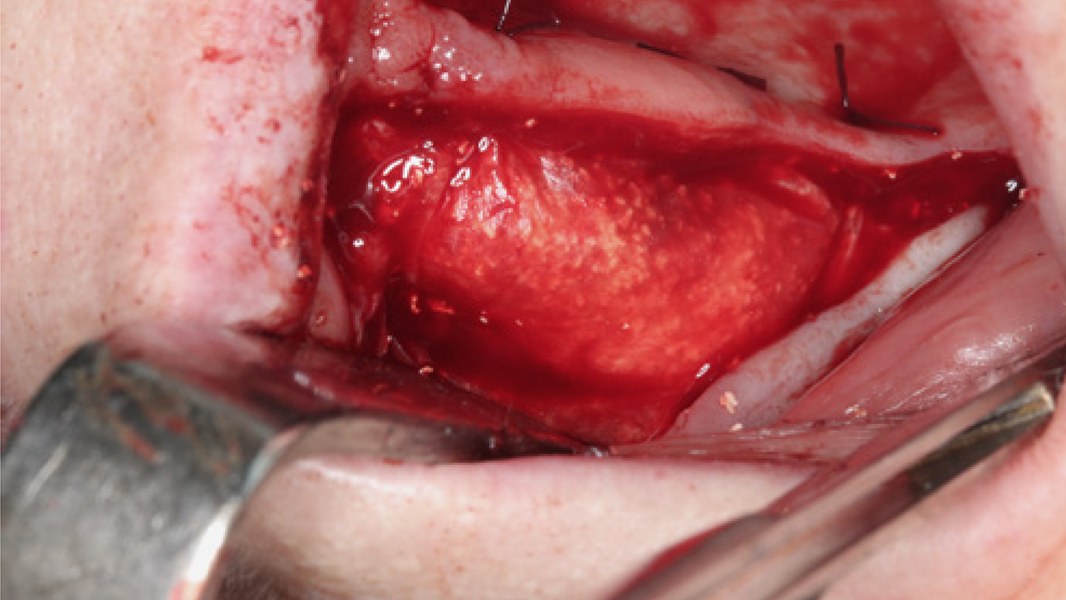
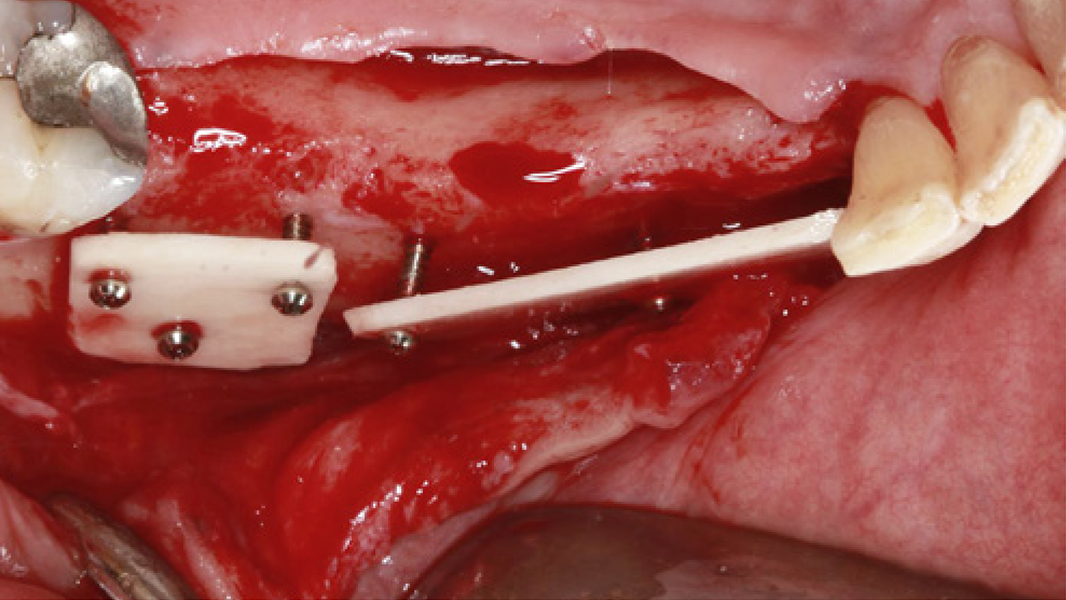
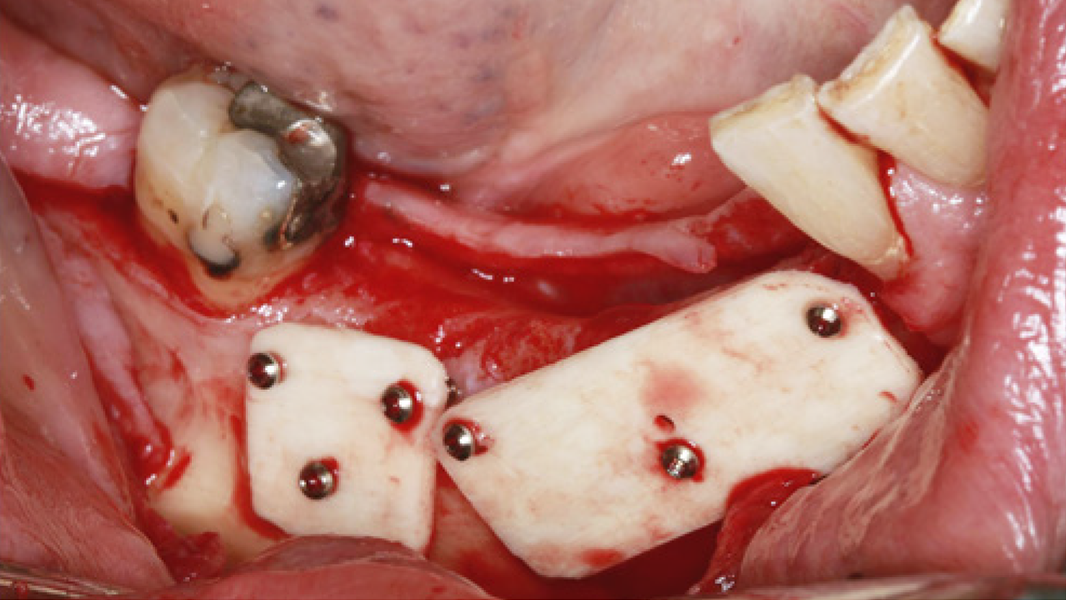
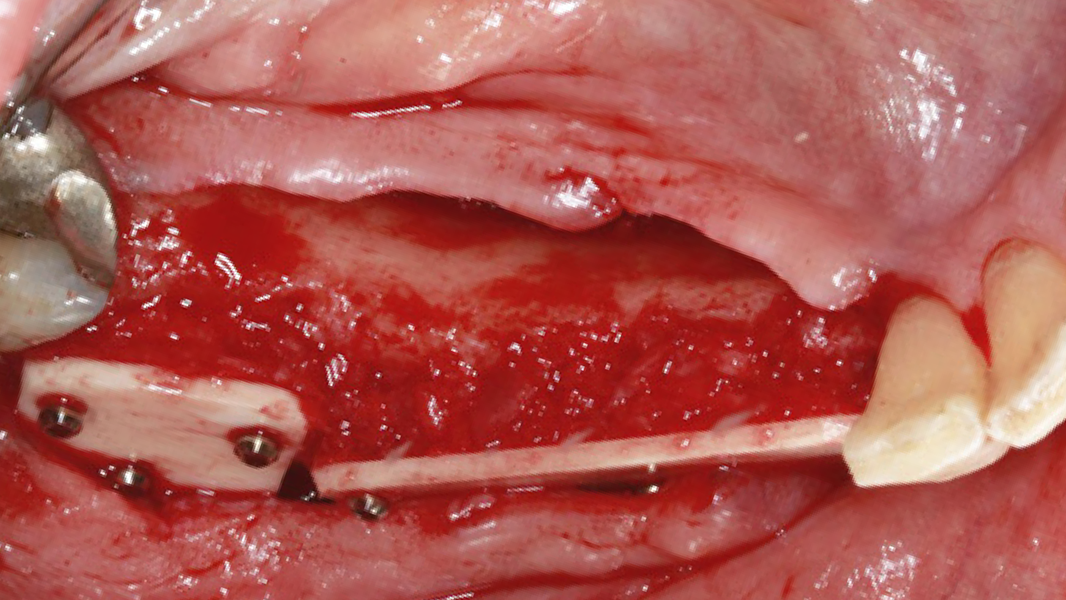
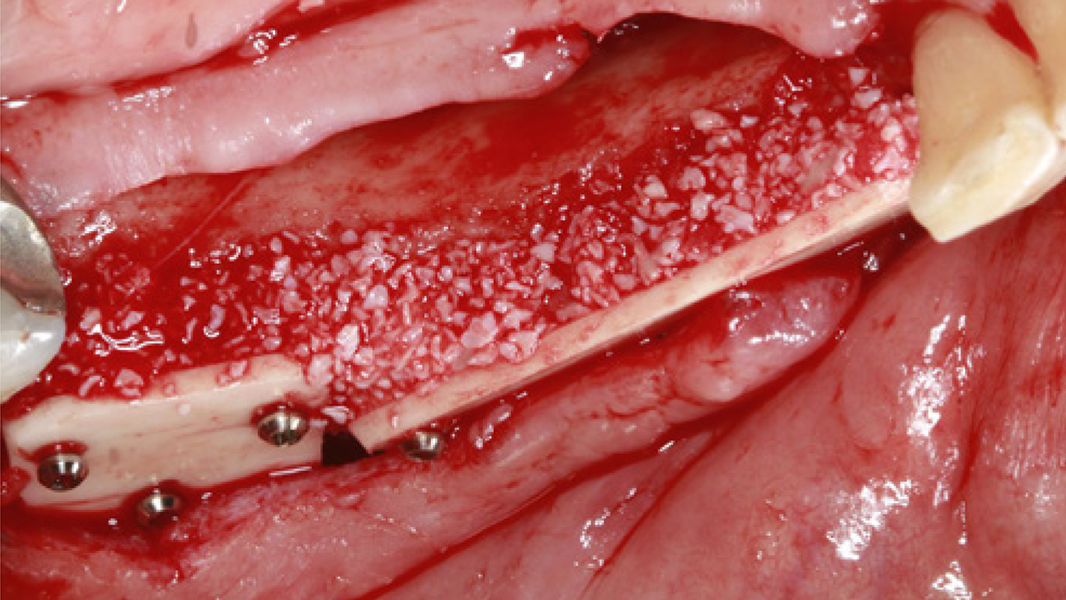
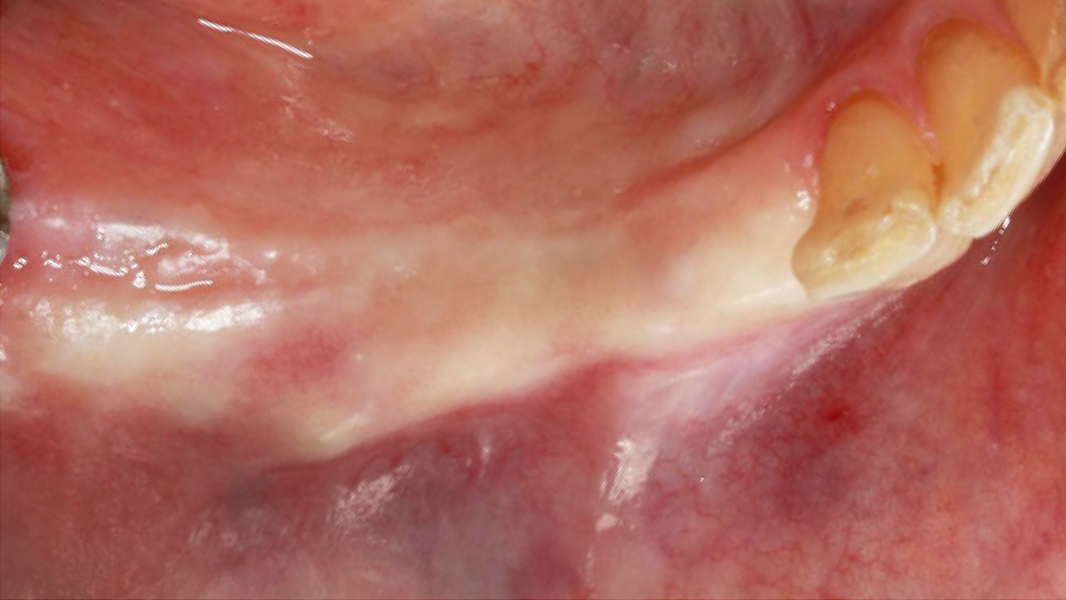
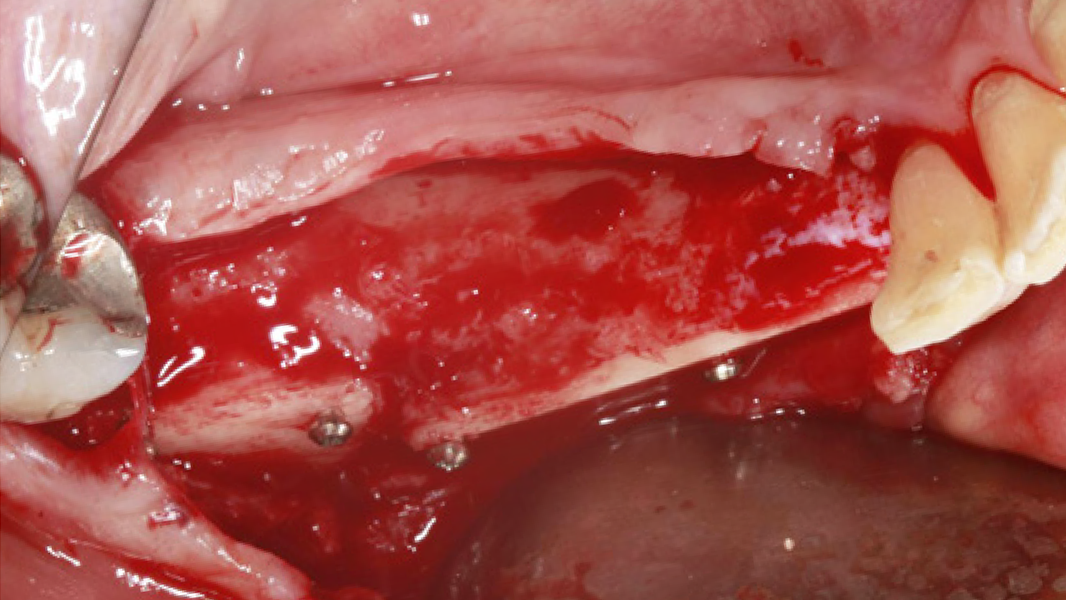
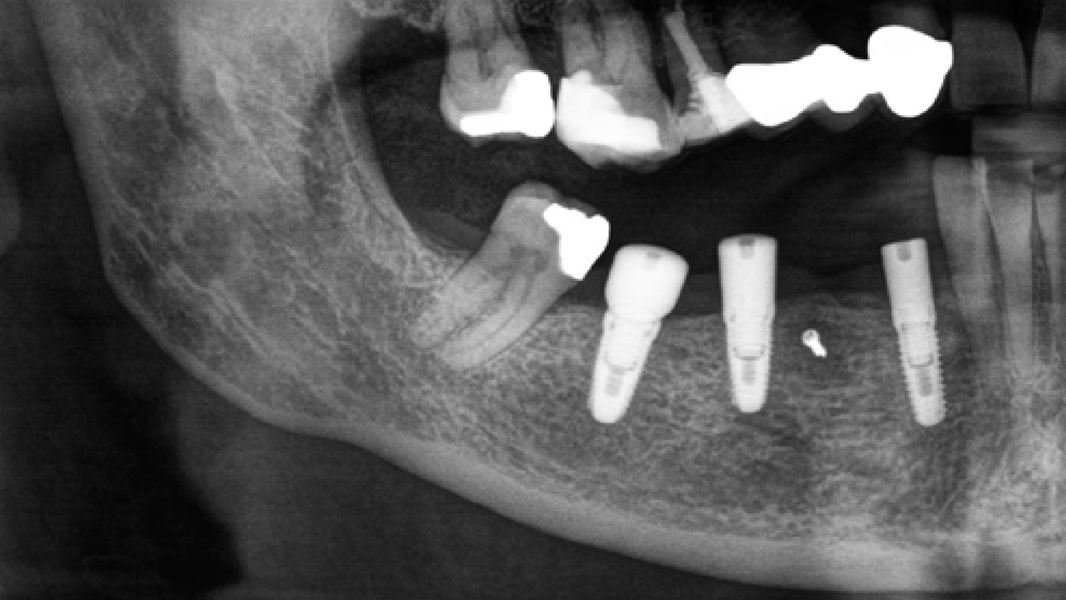
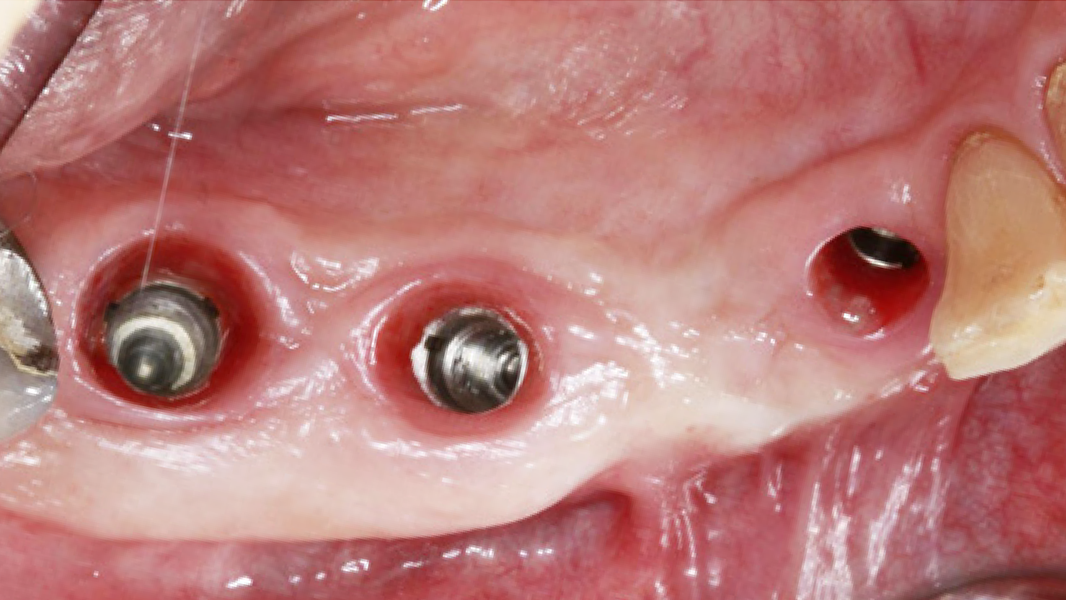
MinerOss® A Portfolio – die allogene Alternative
Schnelle Integration und natürliches Remodelling
MinerOss A Produkte sind ein aus humanem Spenderknochen hergestelltes allogenes Knochenersatzmaterial. Sie werden hauptsächlich aus humanen Femurköpfen von Lebendspendern gewonnen, die eine sorgfältige Spenderauswahl und eine gründliche Prozessierung durch die Cells+Tissuebank Austria (C+TBA) durchlaufen. MinerOss A Produkte sind als spongiöses und kortiko-spongiöses Granulat, als Block, als kortikale Platte oder einer kombinierten Form aus MinerOss A Granulaten und dem Hilfsstoff Natriumhyaluronat (im Folgenden „MinerOss A + HYA“) verfügbar.
Die rein spongiösen Granulate ermöglichen durch eine zügige Remodellierung einen schnellen Knochenaufbau bei eingegrenzten Defekten, wohingegen das kortiko-spongiöse Material beim Aufbau ausgeprägter knöcherner Defekte für eine längere Volumenstabilität sorgt.
Die aktuelle Studienlage zeigt, dass allogene Materialien bezüglich des regenerativen Potenzials und des physiologischen Remodellings dem autologen Knochen ähnlicher sind als Knochenersatzmaterial xenogenen oder synthetischen Ursprungs.1–5
Da durch das geschützte Allotec Verfahren das native Kollagen im Material erhalten bleibt,6, 7 zeigen MinerOss A Produkte eine hohe biologische Regenerationsfähigkeit in Kombination mit einem natürlichen Remodelling- Verhalten.4
Daher sind MinerOss A Produkte eine hervorragende Alternative zur Entnahme patienteneigenen Knochens.
Produktmerkmale
- Geschützter Gewebeverarbeitungsprozess erhält die Gewebeintegrität
- Knochen von Humanspendern (Lebendspender: Femurköpfe; Post-mortem-Spender: Röhrenknochen/Diaphyse)
- Natürliche Knochenzusammensetzung – das native Kollagen bleibt im Material erhalten6, 7
- Hohe biologische Regenerationsfähigkeit und natürliches Remodelling4
- Osteokonduktive Eigenschaften unterstützen den kontrollierten Gewebeumbau
- Haltbarkeit fünf Jahre bei Raumtemperatur (5–30 °C)
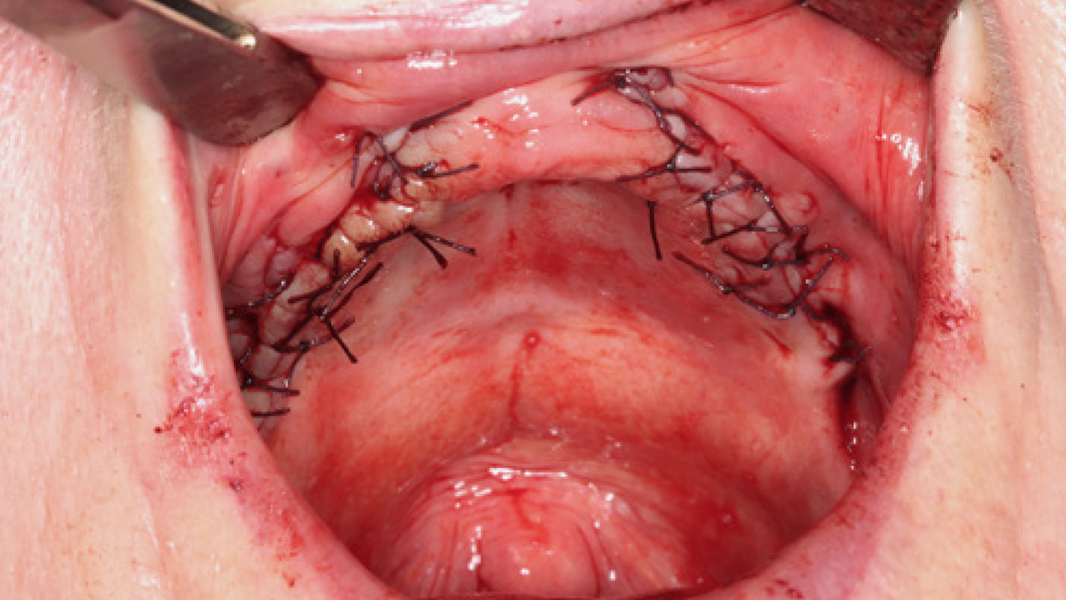
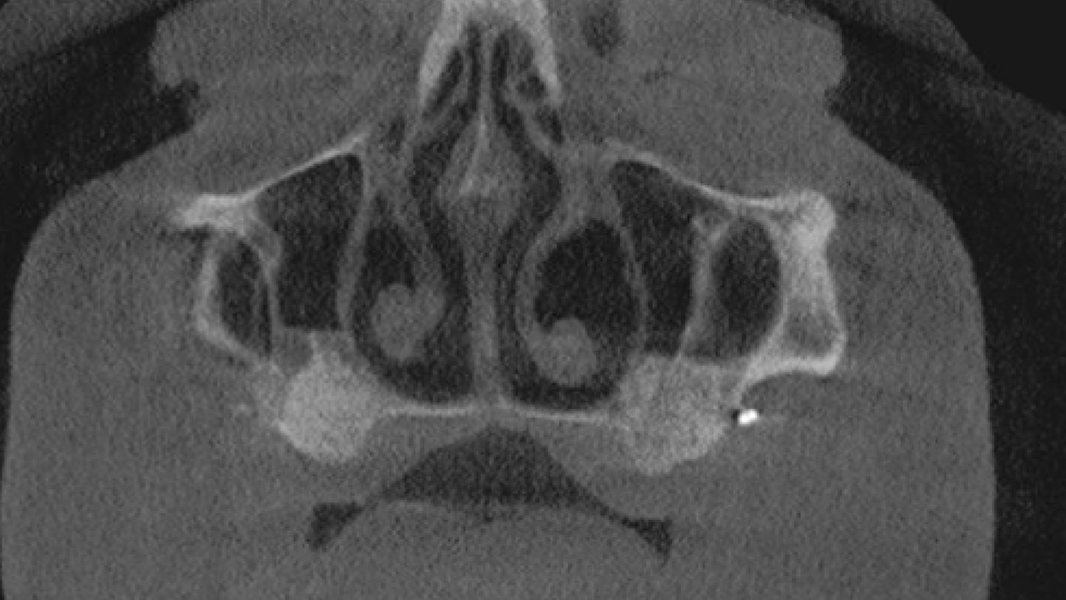
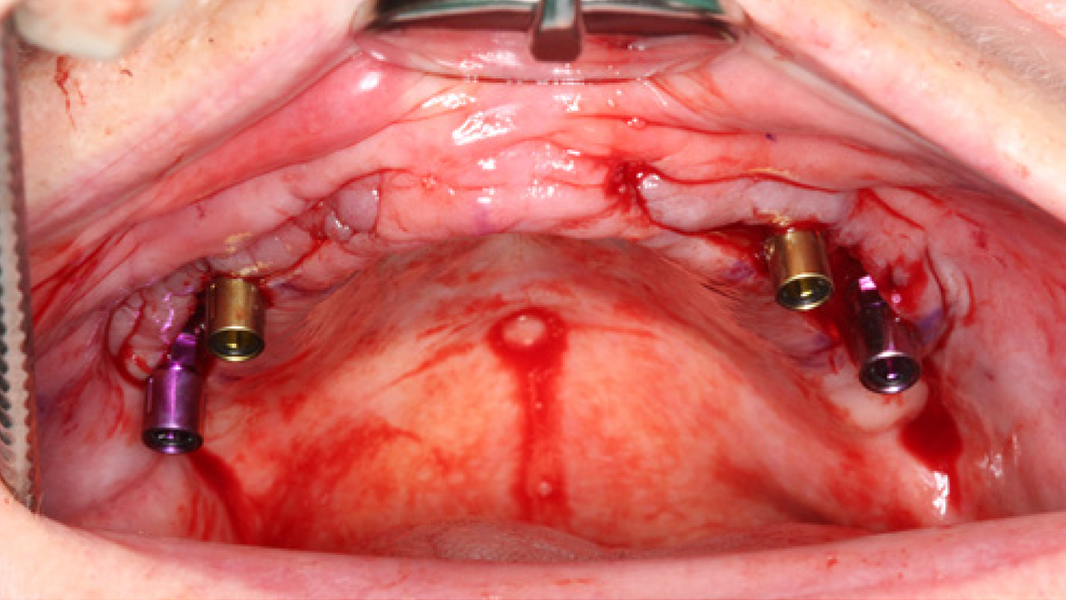
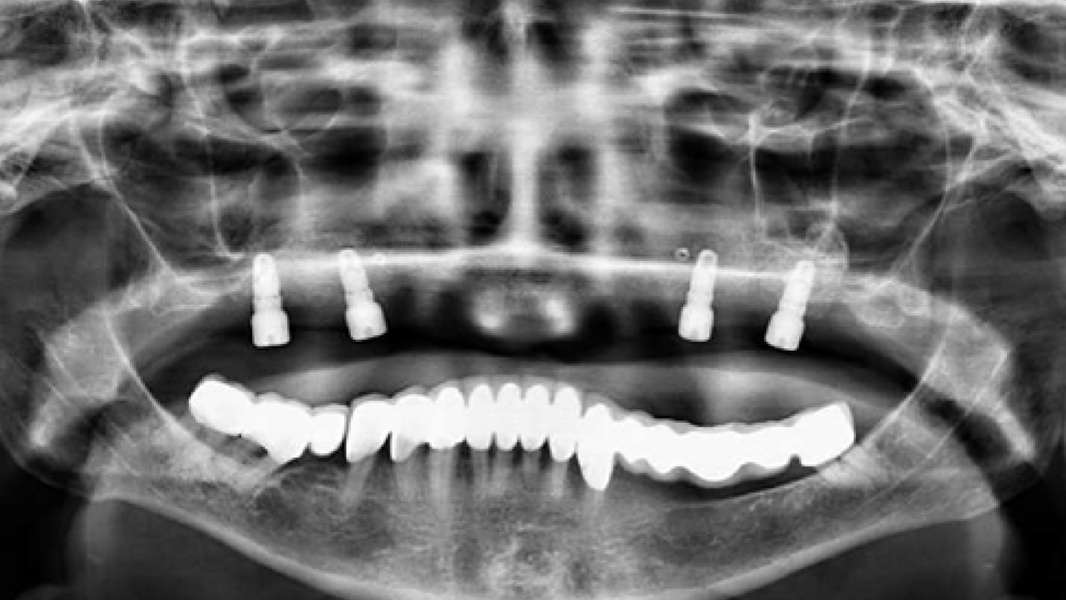
Klinische Erfahrungen
- In einer vergleichbaren klinischen Studie wurde bei Patienten, die mit MinerOss A behandelt wurden, eine signifikant höhere Knochenneubildung nachgewiesen als bei Patienten, die mit bovinem Knochenmineral behandelt wurden.8
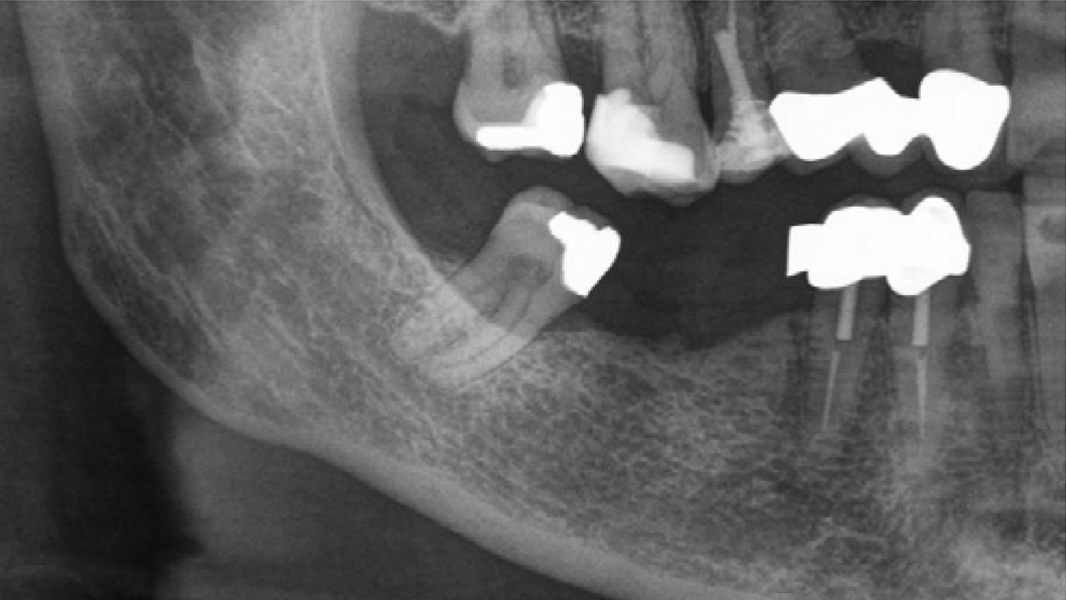
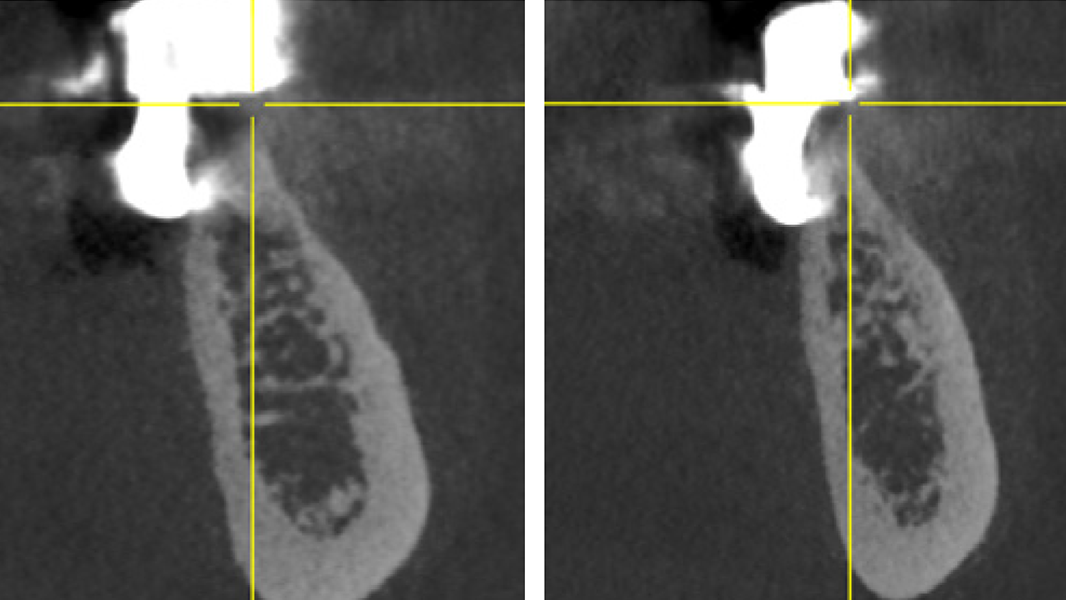
- Die schnelle Remodellierung von MinerOss A verkürzt die Wiedereingliederungszeit und ermöglicht die Implantation nach 3–4 Monaten.9, 10
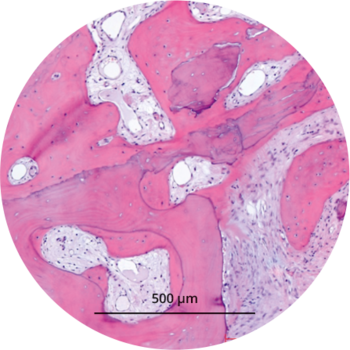
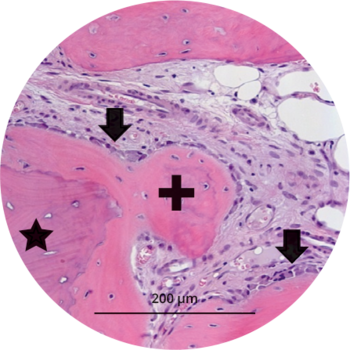
- MinerOss A remodelliert vollständig in den Knochen des Patienten, ohne dass, wie die histologische Kontrolle zeigt, avitale Reste zurückbleiben.3
- MinerOss A stellt eine verlässliche Alternative zu autologem Knochen dar, die eine hervorragende Regenerationsfähigkeit4 und eine geringere Patientenbelastung aufweist.11
Prozessiertes humanes Allograft mit Hyaluronsäure
Eigenschaften
Hyaluronsäure ist ein natürliches Polysaccharid, das in der extrazellulären Matrix verschiedener Gewebe vorkommt und eine entscheidende Rolle bei der Feuchtigkeitsregulation und Zellsignalübertragung spielt.12

Produktmerkmale MinerOss A + HYA
- Innovative Kombination
MinerOss A + HYA kombiniert das allogene Knochengranulat MinerOss A mit dem Hilfsstoff Natriumhyaluronat (NaHyA) – einer Salzform der Hyaluronsäure, die wasserlöslicher und stabiler ist.
- Außergewöhnliche Flüssigkeitsbindungsfähigkeiten
Natriumhyaluronat weist aufgrund der zahlreichen hydrophilen Gruppen in seiner Molekularstruktur, wie Hydroxyl-(-OH) und Carboxylat-(-COO-) Gruppen, außergewöhnliche Flüssigkeitsbindungsfähigkeiten auf.13
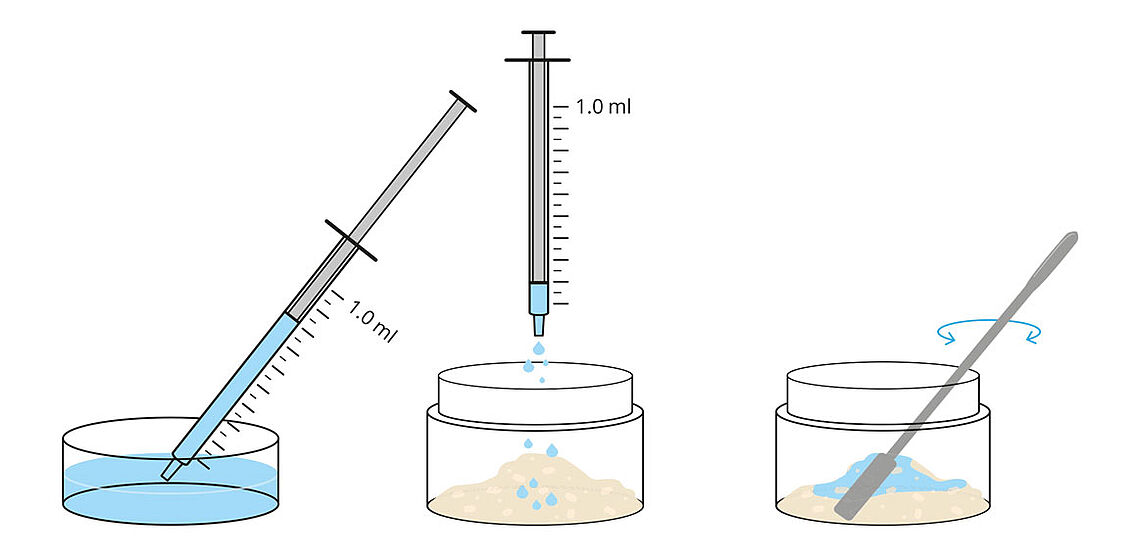
- Verbessertes Handling und präzise Applikation
Wird Natriumhyaluronat dem Knochenersatzmaterial hinzugefügt, ermöglicht es bei Flüssigkeitszufuhr eine mühelose Bereitung von „Sticky Bone“, wodurch die Handhabung des Knochenersatzmaterials bei der Applikation in situ verbessert wird.14, 15
- Einzigartige Komposition
Im Vergleich zu handelsüblichen säurehaltigen Spritzen enthält MinerOss A + HYA bis zu 20-mal mehr Hyaluronsäure, was sich in einer besseren Klebrigkeit und Anpassungsfähigkeit nach der Hydratation niederschlägt.16
Klinische Erfahrungen MinerOss A + HYA
- 85 % der Kliniker bewerteten die Anwendung des „Sticky Bone“ als „einfacher“ oder „viel einfacher“ verglichen mit herkömmlichen Partikeln.14, 17
- Die Präparation des „Sticky Bone“ wurde weitgehend als einfach beschrieben und von den Klinikern mit 8,9 auf einer Skala von 1 (am schwierigsten) bis 10 (am einfachsten) bewertet.14
- Auf einer Skala von 1 bis 10 bewerteten die Kliniker die Heilung des Weichgewebes innerhalb der ersten zwei Wochen mit 8,8 bei den Erstanwendern.14, 17
Der Allotec® Herstellungsprozess
Hohe Sicherheitsstandards
Nach einer sorgfältigen Anamnese des Spenders wird durch eine Reihe stringenter serologischer Tests (u. a. Ausschluss von Hepatitis-B-Virus, Hepatitis-C-Virus, humanes Immundefizienz-Virus, Treponema pallidum (Lues)) in Kombination mit dem Allotec Aufreinigungsverfahren der C+TBA und der Sterilisation durch Gammabestrahlung eine maximal mögliche Sicherheit gewährleistet.
Während des Allotec Aufreinigungsverfahrens werden potenziell vorhandene Viren inaktiviert und Bakterien zerstört. Außerdem werden nicht-kollagene Proteine denaturiert, wodurch eine potenzielle Antigenität eliminiert wird.
Hohe Patientenakzeptanz
Kürzere Behandlungszeit
- Kürzere Operationsdauer – durch den Wegfall eines zweiten chirurgischen Eingriffs für die Transplantatentnahme
- Geringere Komorbidität – keine zusätzlichen postoperativen Schmerzen
- Unbegrenzte Verfügbarkeit – keine Mengenlimitation wie beispielsweise bei intraoraler Entnahmestelle
- Kein klinischer Unterschied in der endgültigen Integration im Vergleich zu autologem Knochen3, 5, 18
Pflichtangaben
MinerOss A wird bei Kleinkindern, Kindern, Jugendlichen und Erwachsenen angewendet zur Transplantation als Ersatz für verloren gegangenes und insuffizientes Gewebe und zum Auffüllen und zur Stabilisierung von Knochendefekten in der Orthopädie, Unfallchirurgie sowie Kiefer und Gesichtschirurgie. Der Einsatz in weiteren Fachdisziplinen ist denkbar.
Mehr Informationen
Referenzen
1 Schmitt et al. Clin Oral Implants Res. 2013, 24, 576.
2 Solakoglu et al. Clin Implant Dent Relat Res. 2019, 21, 1002–1016.
3 Kloss et al. Clin Case Rep. 2020, 8(5):886-893.
4 Wen et al. J Periodontol. 2020. 91(2):215-222.
5 Kloss et al. Clin Oral Implants Res. 2018, 29, 1163.
6 Trajkovski et al. Materials 2018, 11(2):215.
7 Barbeck et al. Materials 2019, 12, 3234.
8 David Chávarri-Prado et al. Int J Periodontics Restorative Dent. 2024, 44(3):309-319.
9 Barone et al. Int J Periodontics Restorative Dent. 2024;44(6):685-696.
10 Kloss et al. Int J Implant Dent. 2024. 10(1):42.
11 Heimes et al. CIDRR. 2024. 26(1):170-182.
12 Garantziotis et al. Matrix Biol. 2019, 78-79:1-10.
13 Necas et al. Vet Med-Czech. 2008, 53(8):397-411.
14 Data on File. Limited Market Release. Users Feedback on Handling and Initial Healing Period 08/2023.
15 Data on File. Limited Market Release. Clinical Case Documentation.
16 Data on File. Marktforschung - Hyaluronsäure Hyaluronsäure-haltige Spritzen 01/2025.
17 Data on File. Entwicklungsbericht: Hyaluronat-Mix Evaluierung Produkteigenschaften 3: „Bone Paste-CTBA“. 03/2024.
18 Tunkel et al. Clin Case Rep. 2020. 9(2):947-959.